Grado Octavo
Nada muere más rápidamente que una idea en una mente cerrada. Pierre Bonnard
archivos para estudiantes suspendidos,
Reacciones Químicas
Una reacción química es un proceso por el cual una o más sustancias, llamadas reactivos, se transforman en otra u otras sustancias con propiedades diferentes, llamadas productos. En una reacción química, los enlaces entre los átomos que forman los reactivos se rompen.
video de experimentos para realizar en las casas.
reaciones quimica para desarrollar en el laboratorio de quimicas.
Taller de Reacciones química
Tipos de reacciones químicas
Es necesario reconocer, que una reacción química sólo puede corresponder a un fenómeno químico que se verifique en condiciones adecuadas; es decir, no se debe proponer una reacción química inventada o que no sea una reacción real. Sin embargo, no siempre es posible predecir sí, al poner en contacto ciertas sustancias, se llevará a cabo la reacción o cuales serán los productos.
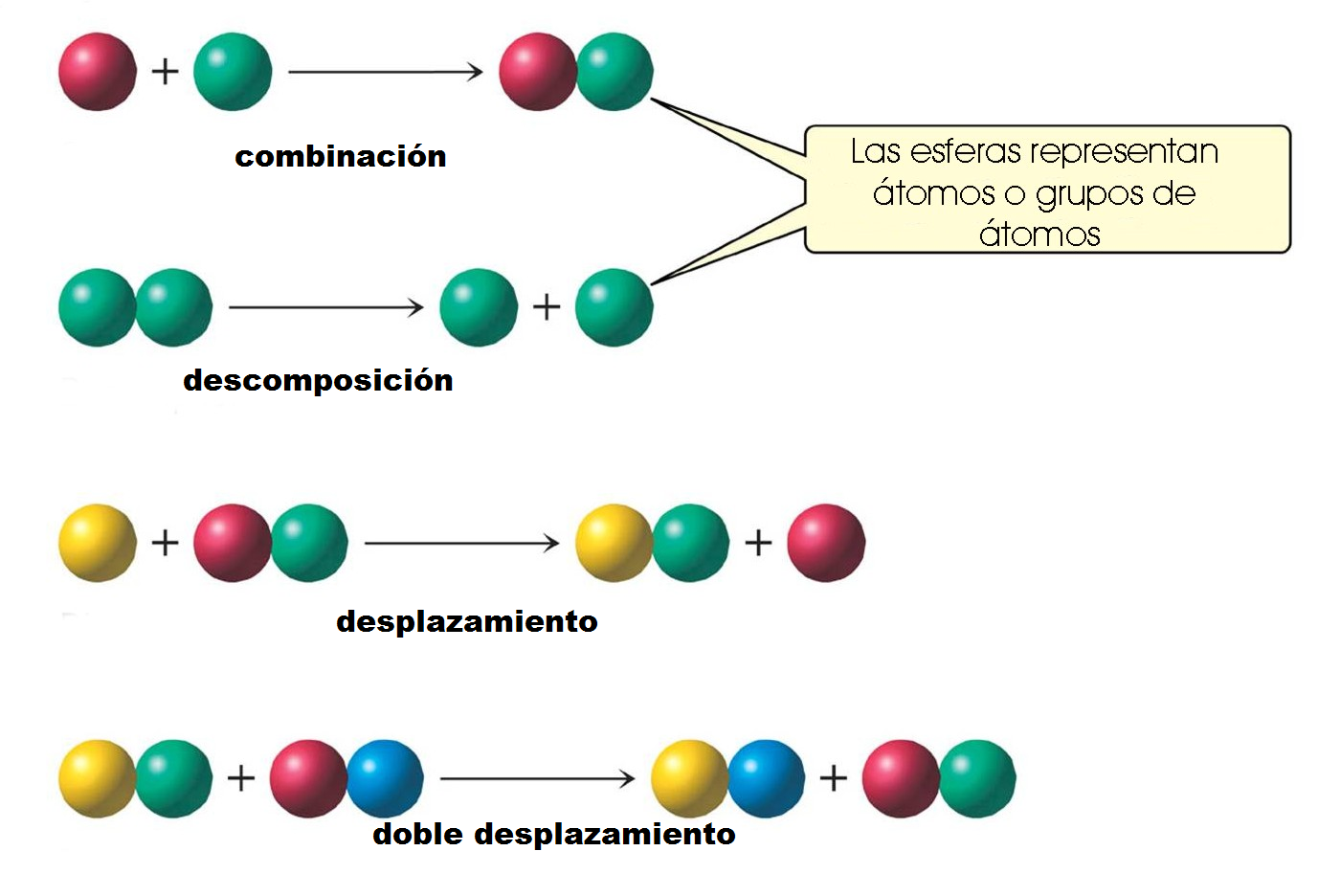
Ahora bien, en miles de experimentos realizados en el mundo, debidamente repetidos y controlados en el laboratorio, las reacciones químicas se pueden clasificar en los siguientes tipos:
De síntesis o combinación
Es un fenómeno químico, y a partir de dos o más sustancias se puede obtener otra (u otras) con propiedades diferentes. Para que tenga lugar, debemos agregar las sustancias a combinar en cantidades perfectamente definidas, y para producirse efectivamente la combinación se necesitará liberar o absorber calor (intercambio de energía).
La combinación del hidrógeno y el oxígeno para producir agua y la del hidrógeno y nitrógeno para producir amoníaco son ejemplos
2H 2 + O 2 -> 2 H 2 O formación de agua
3 H 2 + N 2 -> 2 N H 3 formación de amoníaco
De descomposición
Es un fenómeno químico, y a partir de una sustancia compuesta (formada por dos o más átomos), puedo obtener dos o más sustancias con diferentes propiedades.
Ejemplos: al calentar óxido de mercurio, puedo obtener oxígeno y mercurio; se puede hacer reaccionar el dicromato de amonio para obtener nitrógeno, óxido crómico y agua.
Para que se produzca una combinación o una descomposición es fundamental que en el transcurso de las mismas se libere o absorba energía, ya que sino, ninguna de ellas se producirá. Al final de cualquiera de las dos tendremos sustancias distintas a las originales. Y ha de observarse que no todas las sustancias pueden combinarse entre sí, ni todas pueden ser descompuestas en otras.
De sustitución o de reemplazo
En este caso un elemento sustituye a otro en un compuesto, ejemplos:
Zn + 2HCl --> ZnCl 2 + H 2
Mg + H 2 SO 4 --> Mg SO 4 + H 2
De doble sustitución o de intercambio
En este tipo de reacciones se intercambian los patrones de cada compuestos, ejemplo
2 CuOH + H 2 SO 4 --> Cu 2 SO 4 + 2H 2 O
Reactantes y productos
Para entenderlas y analizarlas, las reacciones químicas se representan, como ya vimos en los ejemplos anteriores, mediante ecuaciones químicas .
Una ecuación química es la representación escrita de una reacción química. En toda reacción química debemos distinguir los reactantes y los productos .
Los reactantes son sustancias que al combinarse entre ellas a través de un proceso llamado reacción química forman otras sustancias diferentes conocidas como productos de la reacción.(Ver: Velocidad de una reacción química )
En una ecuación química, los reactantes y productos se escriben, respectivamente, a la izquierda y a la derecha, separados mediante una flecha. El sentido de la flecha indica el transcurso de la reacción y debe leerse como: da origen a
Reactantes --> dan origen a Productos
Tomaremos como ejemplo el agua, las sustancias reactantes son el hidrógeno (cuya fórmula es H 2 ) y el oxigeno (cuya fórmula es O 2 ), al combinarlas se produce una reacción química y obtenemos como producto el agua:
Dos moléculas de hidrógeno (2H 2 ) reaccionan con una molécula de oxigeno (O 2 ) para formar dos moléculas de agua (2H 2 O).